Taux de mortalité dans PAH/PAV/vPAH

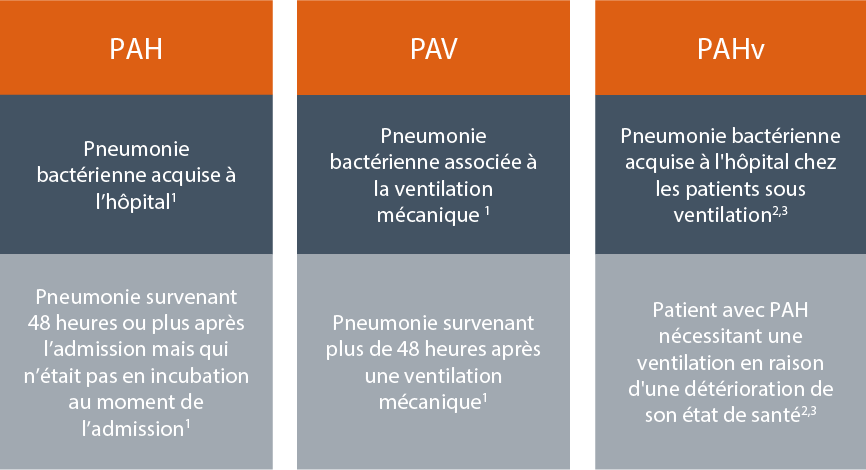
Définitions
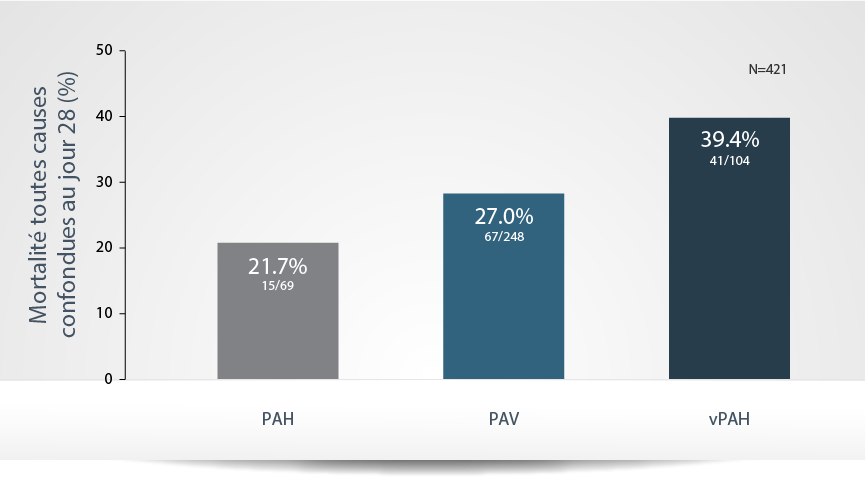
Taux de mortalité chez les patients
atteints de PAH/PAV/vPAH
Dans une étude prospective
La mortalité de toutes causes confondues à 28 jours
par sous-population de patients atteints de
PAH/PAV/vPAH dans AT-USI4,5
Une revue de la littérature ciblée a identifié les prédicteurs de TCM chez les patients atteints de PAH/vPAH
Les patients avec vPAH sont exposés à un risque de mortalité plus élevé que les patients souffrant de PAV4
Description de l’étude2,4:
- Étude prospective sur les épisodes initiaux de pneumonie bactérienne suspectée d’être acquise en USIa
- Les scores APACHE II et SOFA au début de la maladie étaient plus élevés dans le groupe vPAH par rapport aux groupes PAH/PAV
- Les sujets étaient généralement des hommes âgés ayant déjà pris beaucoup d’antibiotiques.
Ensembles de données incluaient les données démographiques des patients ; variables prédictives/de risque pour la TCM (par exemple, score APACHE II de physiologie aiguë et d’évaluation de la santé chronique ; évolution des signes de pneumonie et de l’oxygénation (oxygène inspiré fractionné (FiO2)/tension artérielle d’oxygène (PaO2)) pendant le traitement ; amélioration des symptômes de pneumonie au fil du temps ; les taux de TCM; et les événements indésirables (EI) qui pourraient former un critère d’évaluation de « mortalité plus » (TCM+) (un critère d’évaluation composite de TCM et des EI sélectionnés reflétant la façon dont un patient se sent ou fonctionne)
Pour le nv-PAH, la fréquence initiale et l’évolution des symptômes de la pneumonie confortaient un critère d’évaluation basé sur les symptômes, comme pour le CABP. Dans l’étude Pfizer 311, 95,6 % des patients nv-PAH présentaient ≥2 symptômes au départ (contre 46,8 % pour le PAV). Cependant, le critère d’évaluation précédemment dérivé pour le CABP n’a pas pu être appliqué à l’PAH, car la répartition des symptômes de base entre le CABP et l’PAH n’était pas comparable. Les taux de TCM ont été rapportés pour le nv-PAH, le PAHv et le PAV, différant considérablement au sein et entre les études : par exemple, dans l’étude Pfizer 311, les taux de TCM étaient de 9,8 %, 15,2 % et 12,6 %, respectivement, au jour 28, alors que dans les études ATTAIN, les taux étaient respectivement de 18,8 %, 30,2 % et 26,3 %. Le nombre d’EI vraisemblablement liés à la pneumonie sous-jacente (par exemple, insuffisance respiratoire, empyème) a soutenu l’élaboration d’un critère d’évaluation TCM+.
aLes patients provenaient d’une étude menée dans un seul centre.
APACHE II, Acute Physiological Assessment and Chronic Health Evaluation II; PAH, Pneumonie Acquise à l’Hôpital; PAV, Pneumonie Acquise sous Ventilation; PAHv, Pneumonie Acquise à l’Hôpital sous ventilation; TCM, toute cause de mortalite,USI, unité de soins intensifs, AT, population d’analyse de tous les patients traités; CABP, pneumonie bactérienne acquise dans la communauté.
Bibliographie
- Kalil AC, et al. Clin Infect Dis. 2016;63(5):e61–e111.
- Foundation for the National Institutes of Health. Considerations for clinical trial design for the study of hospital-acquired bacterial pneumonia and ventilator-associated bacterial pneumonia. Foundation for the NIH Biomarkers Consortium HABP/VABP Project Team, May 26, 2017. fnih.org/what-we-do/biomarkers-consortium/programs/ventilator-acquired-bacterial -pneumonia. Accessed December 24, 2024.
- US Department of Health and Human Services. Guidance for Industry Hospital-Acquired Bacterial Pneumonia and Ventilator-Associated Bacterial Pneumonia: Developing Drugs for Treatment. Available at: https://www.hhs.gov/guidance/sites/default/files/hhs-guidance-documents/Hospital-Acquired-Bacterial-Pneumon ia-and-Ventilator-Associated-Bacterial-Pneumonia Developing-Drugs-for-Treatment.pdf. Accessed: December 24, 2024.
- Talbot GH, et al. J Infect Dis. 2019;219(10):1536-1544.
- Talbot GH, et al. (Supplementary material). J Infect Dis. 2019;219(10):1536-1544.
DZ-ZER-00040. Date d’expiration : 24-1-2026