Critères d’évaluation
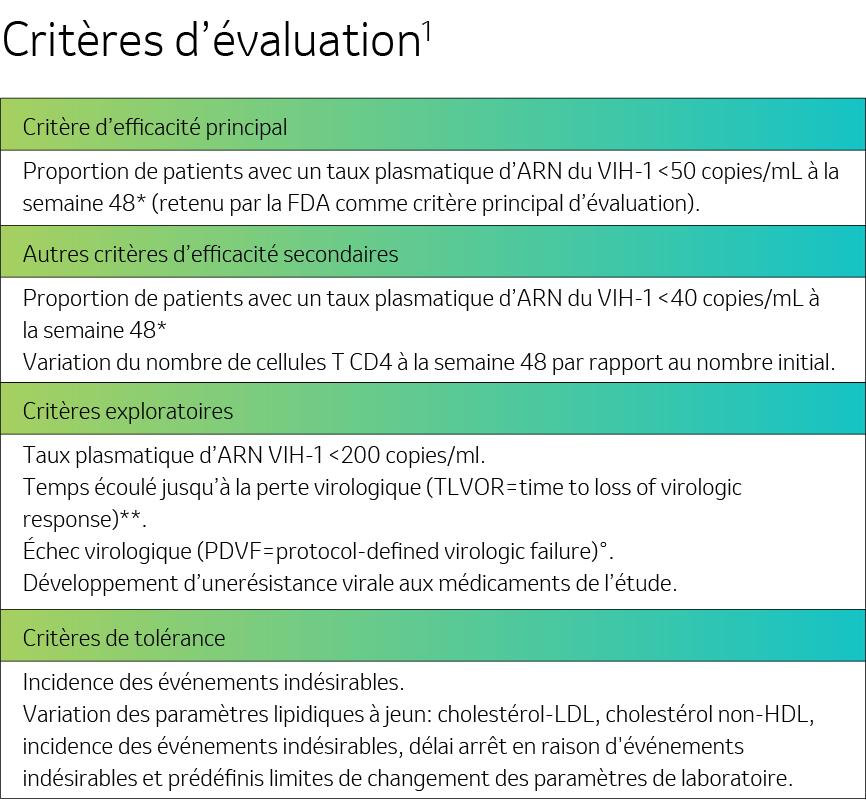
ARN = acide ribonucléique.
*Tel que défini par US Food Drug Administration (FDA) snapshot algorithm.
**Pour les sujets dont les taux d’ARN du VIH-1 confirmés étaient inférieurs à 50 copies/mL (sur deux visites consécutives), TLOVR est le temps entre le jour 1 et la première de deux valeurs consécutives (à au moins une semaine d’intervalle)
au-dessusde 50 copies/mL ou une perte de suivi après avoir atteint un taux d’ARN du VIH-1 confirmé inférieur à 50 copies/mL. Pour les sujets qui atteignent et maintiennent un taux d’ARN du VIH-1 <50 copies/mL, TLOVR est censuré au moment de la dernière visite disponible. Pour les sujets n’ayant jamais atteint des niveaux confirmés d’ARN du VIH-1 inférieurs à 50 copies/mL (sur deux visites consécutives), TLOVR est le temps 0.2
°L’échec virologique défini au protocole consistait en un rebond virologique (confirmation d’un taux d’ARN-VIH-1 ≥ 50 copies/mL après une réponse initiale correspondant à un taux d’ARN-VIH-1 <50 copies/mL à tout moment pendant l’étude) ou une non-réponse (confirmation d’un taux d’ARN-VIH-1 ≥ 200 copies/mL à la semaine 24 ou 36 ou confirmation d’un taux d’ARN-VIH-1 ≥50 copies/mL à la semaine 48). Les patients répondant aux critères du PDVF étaient sortis de l’étude, indépendamment de leur niveau d’observance au traitement de l’étude.
#Les analyses statistiques étaient prédéfinies uniquement pour le cholestérol-LDL et le cholestérol non-HDL.1,2
Bibliographie:
- Molina JM, Squires K, Sax PE, et al. Doravirine versus ritonavir-boosted darunavir in antiretroviral-naive adults with HIV-1 (DRIVE-FORWARD): 48-week results of a randomised, double-blind, phase 3, non-inferiority trial. Lancet HIV. 2018;5(5):e211-e220.
- Molina JM, Squires K, Sax PE, et al. Doravirine versus ritonavir-boosted darunavir in antiretroviral-naive adults with HIV-1 (DRIVE-FORWARD): 96-week results of a randomised, double-blind, non-inferiority, phase 3 trial. Lancet HIV. 2020;7(1):e16-e26.
DZ-DOR-00009. Date d’expiration: 1-10-2026